
做IgE 相关研究时,你是否常遇到这些难题?测血清总 IgE 总因标准品不准导致数据反复;想验证过敏级联反应关键步骤,却找不到能精准靶向 FcεRI 受体的抗体;甚至探索 IgE 与心血管疾病的关联时,连基础机制的实验切入点都抓不准?
其实突破这些困境的核心,就藏在对IgE 的精准认知与高特异性研究工具的选择里。这种在人体免疫球蛋白中含量最低(仅占 0.001%)、半衰期短(血液中 2-5 天,结合受体后延长),却能串联过敏反应、寄生虫感染甚至心血管风险的分子,正是打开研究突破口的关键。下面我们从 “机制痛点” 到 “工具解决方案”,帮你把 IgE 研究的堵点逐个打通。
先搞懂:IgE到底是种“什么样的分子”?
人IgE(免疫球蛋白 E)和 IgG、IgA 等一样,由两条重链和两条轻链组成,但它的 “独特性” 恰恰是研究的核心——重链是 ε 链(IgE 专属),带有 4 个恒定区(Cε1~Cε4),没有铰链区,且含较多半胱氨酸和甲硫氨酸。这种结构让它能牢牢结合细胞表面的受体,也决定了它的 “亲细胞” 特性。
从产生部位来看,IgE 主要来自鼻咽部、扁桃体、支气管、胃肠等粘膜固有层的浆细胞——这些地方正是过敏原最易入侵、I 型变态反应最常发生的 “主战场”。也正因如此,血清总 IgE 检测才成为区分过敏性疾病与其他相似症状疾病的关键手段:比如同样是咳嗽,测出血清 IgE 升高,更可能指向过敏性哮喘,而非普通炎症。
IgE如何“搞事情”?从过敏反应到心血管风险的机制拆解
IgE 的作用离不开两种关键受体——高亲和力受体 FcεRI(主要在肥大细胞、嗜碱性细胞表面)和低亲和力受体 CD23(多在 B 细胞、上皮细胞表面)。搞懂这两种受体介导的机制,就能抓住实验设计的核心。
1. 过敏级联反应:这 3 个关键环节,实验别漏检!
过敏原想要引发过敏症状,需要经过一套“完整流程”,每个步骤都有可检测的关键指标,帮你验证实验逻辑(见图 1:过敏级联反应):
第一步:过敏原突破屏障,唤醒“炎症信号”
过敏原通过受损的上皮屏障进入机体后,会触发上皮细胞释放IL-25、IL-33、TSLP 这三种细胞因子——这是 “过敏启动信号”,若检测不到这些因子,后续反应就无从谈起,实验中可通过 ELISA 或 WB 验证其表达量。
第二步:Th2 细胞 “指挥” B 细胞产 IgE
上述细胞因子会激活Ⅱ 型先天淋巴样细胞(ILC2)和树突状细胞(DC),分泌 IL-4、IL-5、IL-13,这些 Ⅱ 型细胞因子会推动 Th0 细胞向 Th2 细胞分化。关键一步来了:Th2 细胞分泌的 IL-4、IL-13 会诱导 B 细胞发生 “类别转换”(从产生 IgM 转为产生 IgE),最终生成过敏原特异性 IgE——这一步可通过检测 B 细胞的 IgE 抗体分泌量,验证 Th2 细胞的调控作用。
第三步:IgE “引爆” 过敏症状
生成的IgE 会稳定结合在肥大细胞、嗜碱性细胞表面的 FcεRI 受体上。当过敏原再次入侵时,会快速结合这些 “预结合” 的 IgE,触发细胞脱颗粒,释放组胺、前列腺素、半胱氨酰白三烯等可溶性介质——这就是过敏症状(如打喷嚏、皮肤瘙痒)的直接原因,实验中可通过检测介质释放量,判断过敏反应的激活程度。
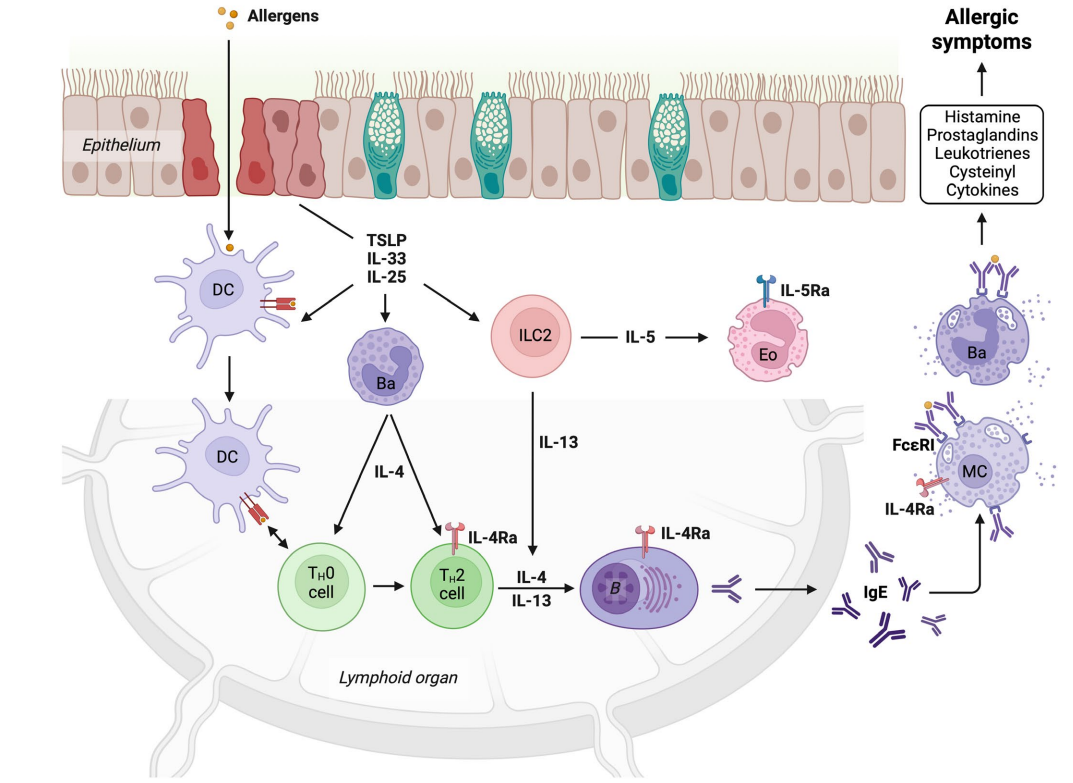
图1. 过敏级联反应
参考来源:Immunol Rev. 2024 Nov;328(1):387-411. doi: 10.1111/imr.13380.
2. CD23 受体:既是 “抗原提呈助手”,也是 “过敏抑制剂”
低亲和力受体CD23(属于 C 型凝集素超家族)的作用很 “双面”,实验中可根据需求针对性利用(见图 2:IgE 介导的过敏原提呈):
细胞表面CD23:帮抗原提呈更高效
B 细胞、上皮细胞表面的 CD23 会与 IgE 形成复合物,随后通过 “复合物内化” 的方式,把过敏原更精准地呈递给 DC 细胞和 Th2 细胞,进而增强免疫反应 —— 做 “抗原提呈机制” 研究时,用 CD23 特异性抗体标记,能清晰定位这一过程。
可溶性CD23(sCD23):抑制过敏的 “好帮手”
游离的sCD23 会竞争性结合 IgE,阻止 IgE 与 FcεRI 结合,从而减少过敏反应的激活 —— 筛选抗过敏药物时,sCD23 的表达量可作为 “药效指标”:药物处理后 sCD23 升高,可能意味着抗过敏效果更好。
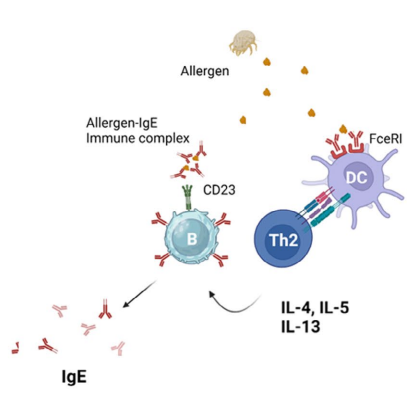
图2. IgE介导的过敏原提呈
参考来源:Immunol Rev. 2024 Nov;328(1):314-333. doi: 10.1111/imr.13386.
3. 不止过敏!IgE 还是心血管疾病的 “隐藏风险因子”
近几年《Immunol Rev.》等期刊的研究证实:血清 IgE 水平升高是心血管疾病的独立危险因素,它会通过 “免疫 - 炎症” 通路推动动脉粥样硬化(AS)发生发展:当 IgE 与肥大细胞、嗜碱性细胞表面的 FcεRI 结合后,会激活细胞释放组胺、IL-6 等炎症介质 —— 组胺会损伤血管内皮细胞,让脂质更易沉积;IL-6 则会加速动脉粥样硬化斑块的形成,还会让斑块 “变脆”(降低稳定性),增加心梗、脑梗等心血管事件的风险。对做 “免疫 - 心血管交叉研究” 的人来说,这是个新方向:靶向 IgE 或 FcεRI,或许能找到防治动脉粥样硬化的新靶点。
IgE研究“少走弯路”的关键:选对高特异性工具
Bioss 作为全球领先的抗体与蛋白研发专家,针对 IgE 研究的核心需求(定量检测、功能验证、体内实验、IVD 开发),打造了一系列 “解决痛点型” 工具,帮你省去 “试错时间”,直接拿到可靠数据。
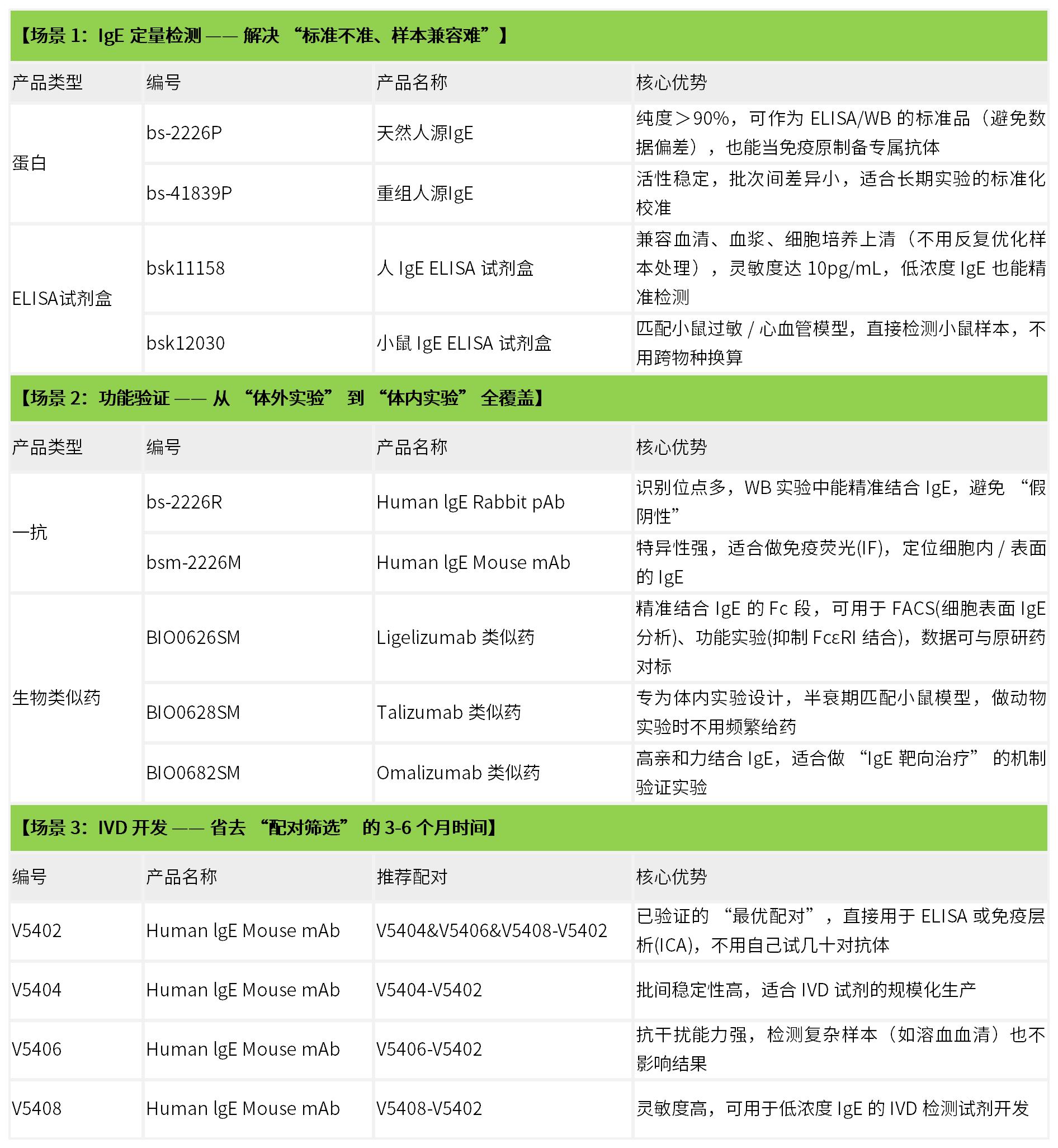
无论是做基础机制研究(过敏/ 心血管关联),还是推进 IVD 或药物开发,选对 IgE 研究工具,就能避开 “数据不准、重复难、进度慢” 的坑——这也是让你的 IgE 研究从 “跟风” 到 “脱颖而出” 的关键。
